キュライオではクライオ電子顕微鏡による構造解析をベースとした創薬事業を展開しております。

クライオ電子顕微鏡とは?
クライオ電子顕微鏡単粒子解析法とは、2017年にノーベル化学賞が授与された、近年急激に注目が高まっている電子顕微鏡による構造解析の手法の一つです。
従来までの創薬研究(医薬品の研究)は、構造が分からないタンパク質に対してヒットするものが現れるまで何百万回の試行錯誤(何百万個の化合物評価)を要し非常に長い時間と大きなコストがかかっておりました。
クライオ電子顕微鏡を用いることによって、従来の解析手法であったX線構造解析で困難だったタンパク質の多くにおいて構造解析が可能となり、確実に構造解析ができるタンパク質が増えるため、新たな創薬領域が大きく拡がっていくことが期待されております。

現在、弊社ではThermo Fisher Scientific社製のクライオ電子顕微鏡 Talos Arctica G2、Titan Krios G3i、また最新鋭機に当たる Titan Krios G4を駆使し創薬研究を行っております。
-

Talos Arctica G2 -

Titan Krios G3i -

Titan Krios G4
電子顕微鏡の種類
 透過電子顕微鏡(TEM) – Transmission Electron Microscopy
透過電子顕微鏡(TEM) – Transmission Electron Microscopy
- 電子線をあて、透過してきた電子を観察
- 試料の構成成分により透過電子の密度が変化
- 加速電圧300kVの電子線波長は0.002nm
 走査電子顕微鏡(SEM) – Scanning Electron Microscopy
走査電子顕微鏡(SEM) – Scanning Electron Microscopy
- 電子線で試料表面をスキャン
- 二次電子や反射電子の信号を元に像を作成
![]()

クライオ電子顕微鏡 (Cryogenic Electron Microscopy)
Cryogenicとはギリシャ語で寒冷を表す「cryos」と生み出すの意味を持つ「gennese」を組み合わせた、低温を発生させる技術を指します。
Cryogenic電子顕微鏡、通称クライオ電顕(CryoEM)とは液体窒素(-196℃)冷却下でタンパク質などの生体分子に対して電子線を照射し、試料の観察を行うための装置、透過電子顕微鏡(TEM)をベースとした新手法になります。タンパク質の立体構造を高分解能で決定する手法として、検出器などにおいて目覚ましい技術革新を遂げており、2017年に、その開発に貢献した海外の研究者三名にノーベル化学賞が贈られました。
この新手法は1995年には100kDa*¹以上までの分子であれば構造解析が可能であることが理論的に示され、その後、特に2015年以降活発に研究開発が行われ、近年の“Resolution Revolution”(分解能革命)により1.5Å*²以下の分解能で分子構造の解明が可能に。また、最近では約50~60kDa近辺の分子の構造解析が可能となっています。
![]()
分解能別:CryoEMによるタンパク質の解析件数推移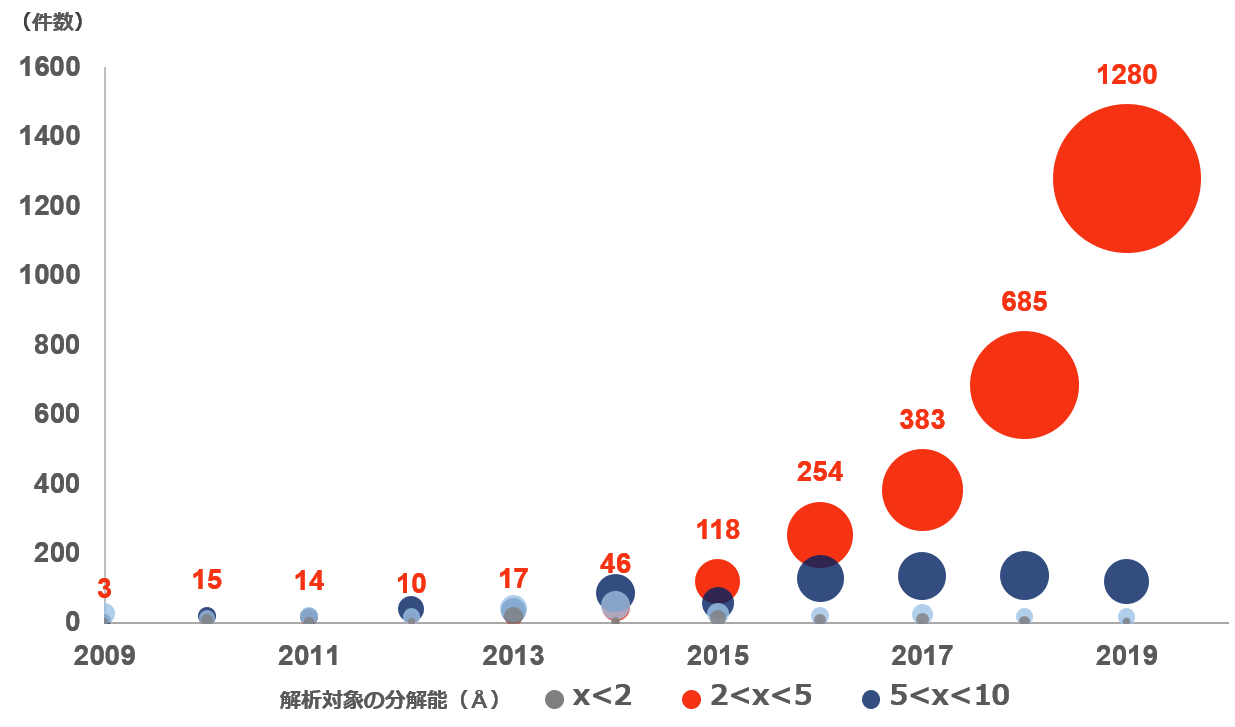
分解能2Å-5Åの件数が過去5年で急激に増加していることが確認できる。
Source: Protein Data Bank Japanの情報を元に当社で作成
- *¹ Da(ダルトン): 質量を表す単位、12C原子の質量の1/12を1とする。kDa(キロダルトン)
- *² Å(オングストローム):1Åは10−10m = 0.1ナノメートル(nm) = 100ピコメートル(pm) と定義されている
単粒子解析法
単粒子解析法(single particle analysis, SPA)とは液体窒素温度条件下(クライオ)において透過型電子顕微鏡を用いてタンパク質分子の像(写真)を多数撮影し、それらの平均化を行い3次元構造へと再構築する手法です。多数の撮影画像の加算平均をとることでノイズを低減し、2Dでの平均化、3D構築での平均化を通して観察対象タンパク質の分解能を向上させることが可能。また、特定ではなく多数のタンパク質から画像を取得するため、生物試料特有の電子線によるダメージに弱いといった問題点も克服されている。
クライオ電子顕微鏡単粒子解析法の強み
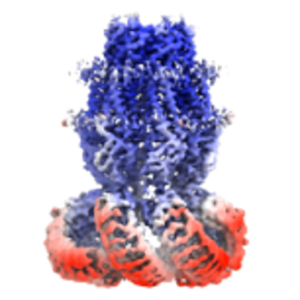
CryoEMの特徴・メリット
- 標的の結晶化が不要
- 生体内に近い環境を維持
- 複数のサブユニットを含む大きな分子に対応
- 原子レベルでの構造観察が可能
- 機能状態に応じて実験条件を変更可能
創薬での強み・得意分野
- 生体内に近い環境で標的の構造解析が可能
- 結晶化が困難であった複合体や膜貫通タンパクなども観察が可能
- より多くのタンパク質の構造解析が可能となる

